DNA - DESOXYRIBONUKLEINSÄURE
Desoxyribonukleinsäure (englisch desoxyribonucleic acid) - besteht aus zwei Polynukleotidketten, die in Form einer Doppelhelix ineinander verschlungen sind.
Es gibt vier Nukleotide (Adenin, Cytosin, Guanin, Thymin - A, C, G, T). Jeweils drei benachbarte Nukleotide kodieren eine der 20 Aminosäuren, die wiederum Gene kodieren.
Beim Menschen ist der Großteil der Gene auf der DNA in Chromosomen organisiert und befindet sich im Zellkern (nukleäre DNA).
Alle Testmethoden in der Blutbank basieren auf dieser DNA. Im Blut findet man sie nur in den weißen Zellen (Leukozyten - Thrombozyten und Erythrozyten sind in der Regel kernlos).
Um eine genetische Untersuchung machen zu können, müssen zuerst die Leukozyten aus dem Blut separiert werden und dann aus den Leukozyten wird die DNA isoliert. Leukozyten lassen sich ebenfalls aus der Milz und den Lymphknoten isolieren.
Anders als in der Forensik, funktionieren unsere Methoden nur mit größeren Mengen DNA - ein Blutstropfen reicht bei uns nicht aus - wir brauchen zumindest einen Milliliter Blut (nur EDTA - Heparin hemmt molekulargenetische Tests).
Allerdings lässt sich auch aus den Epithelzellen der Mundschleimhaut (Abstrich mit sterilem Wattestäbchen) genug DNA isolieren um eine Typisierung zu machen.
Die Extraktion von fetaler DNA aus dem Blut der Schwangeren, um um bestimmte Merkmale zu bestimmen, ist eine relativ junge Methode der nicht-invasiven Fetaldiagnostik.
By brian0918&#153 on wikipedia.de; - Own work
HLA - Humanes Leukozytenantigen System
HLA (human leukocyte antigen) sind Oberflächenproteine, die auf den meisten kernhaltigen Zellen exprimiert werden.
Die wichtigsten HLA-Merkmale, die auch Histokompatibilitätsantigene oder Transplantationsantigene genannt werden, sind in Klasse I und Klasse II eingeteilt.
Der HLA Genkomplex liegt auf dem Chromosom 6 und enthält ca. 200 Gene, von denen nur etwa 40 an der Immunantwort beteiligt sind. Die klassischen HLA-Antigene definieren das immunologische "selbst". Sie zeichnen sich durch einen sehr hohen Polymorphismus aus - das bedeutet die Gene können viele unterschiedliche Ausprägungen haben.
Man teilt diese Gene in zwei Hauptgruppen ein:
HLA Klasse I:
Es gibt ca. 20 unterschiedliche Klasse I Gene, aber nur die "klassischen" HLA-A, -B, -C Moleküle spielen immunologisch eine relevante Rolle. Sie befinden sich auf allen kernhaltigen Zellen und Thrombozyten. Wird eine solche Zelle infiziert, präsentiert sie innerhalb des HLA-Komplexes ein Peptid des "Angreifers". Dieses Peptid in Verbindung mit dem HLA-Komplex aktiviert spezielle zytotoxische Immunzellen (T8-Zellen), die die infizierte Zelle direkt zerstören können. T-Zellen, die in Verbindung mit Klasse I Antigenen aktiviert werden, tragen meistens das CD8 Oberflächenantigen.
Erythrozyten, Spermien und die meisten Nervenzellen exprimieren keine MHC Moleküle (weder MHC I noch MHC II).
Jeder Mensch bekommt jeweils drei HLA-Klasse I Moleküle von der Mutter und drei vom Vater. So dass in der Regel sechs Klasse I Moleküle auf allen kernhaltigen Zellen exprimiert werden.
Die drei Haupt-Gene der Klasse I (A, B, C) kommen zusammen auf ca. 26.610 Allele. Davon machen HLA-A Allele 8.098, HLA-B 9.656 und HLA-C 8.084 aus. Diese Zahl wächst beinahe täglich, aber die Datenbank wird vier Mal im Jahr aktualisiert.
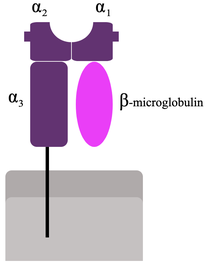
MHC I Aufbau:
HLA Klasse I Gene (A, B, C) kodieren die α Polypeptidkette des MHC I (Major Histocomatibility Complex I). Die β Kette besteht aus dem beta2-Mikroglobulin, welches auf dem Chromosom 15 kodiert ist.
Die α-Kette ist die funktionelle Einheit und besteht aus 5 Domänen:
- α1 und α2 bilden die Antigenbindungsgrube
- α3 ist eine immunoglobulin-like domain
- die 4. Domäne ist die Transmembranregion
- die 5. Domäne ist der zytoplasmatischer Fortsatz
Die Antigenbindungsgrube zwischen a1 und a2 Domänen wird im RER mit Peptiden aus 8-10 Aminosäuren beladen und an der Zelloberfläche präsentiert.
Von User atropos235 on en.wikipedia - Eigenes Werk, CC BY 2.5
HLA Klasse II:
Klasse II Antigene befinden sich überwiegend auf "professionellen" antigen-präsentierenden Zellen (B-Zellen, Makrophagen, Langerhans-Zellen: alles Immunabwehrzellen) und aktivieren T-Helferzellen, die das CD4 Oberflächenantigen tragen. Durch Interferon-γ kann die Expression von HLA Klasse II Antigenen auch auf anderen Zellen induziert werden. Aus diesem Grund spielen auch Klasse II Antigene bei Transplantationen eine relevante Rolle.
Die Bezeichnung der Klasse II Gene besteht aus drei Buchstaben: D für die Klasse, P, Q oder R für die Familie und A oder B für die Kette. Z.Bsp.: DQA, DRB, DPB. Fehlt der dritte Buchstabe, handelt es sich wahrscheinlich um die β Kette.
Durch den Aufbau der Moleküle aus zwei getrennten Ketten ist die Variabilität der Klasse II Moleküle größer als die der Klasse I. Da jedes Molekül aus einer beliebigen Kombination von α- und β-Kette besteht, können zwölf unterschiedliche Klasse II Moleküle gebildet werden.
Die Anzahl der Klasse II Allele ist mit ca. 11.398 deutlich geringer. Bei HLA-DRB1 sind es 3.628 HLA-DQB1 2510 und DPB1 2.486.
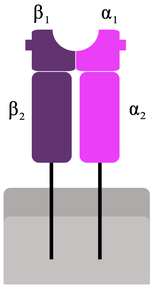
MHC II Aufbau:
Die Klasse II Gene (DQ, DR und DP) kodieren die α und β Polypeptidketten der MHC II Moleküle.
Jede α und β Kette besteht aus vier Domänen:
- α1 und β1 bilden gemeinsam die Antigenbindungsgrube
- α2 und β2 sind immunoglobulin-like domains
- 3. Domäne ist die Transmembranregion
- 4. Domäne ist der zytoplasmatische Fortsatz
Die Antigenbindungsgrube der Klasse II Moleküle präsentiert fremde Peptide von 13-18 Aminosäuren und wird in den Phagolysosomen beladen.
Von User atropos235 on en.wikipedia - Eigenes Werk, CC BY 2.5
Die Benennung von HLA-Antigenen folgt genauen Regeln:
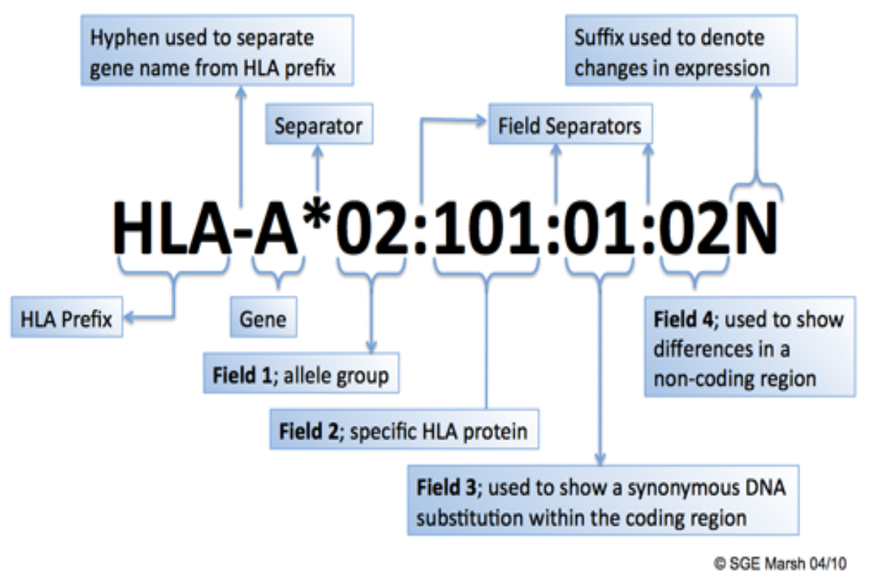
Obwohl bei der Organtransplantation bereits die "high resolution" oder 2-Feld Typisierung möglich ist, wird bei der Allokation nur das serologische Äquivalent berücksichtigt. Die "Übersetzung" der Allele in serologische Äqivalente kommt aus der Zeit, wo nur Antikörper zur Typisierung zur Verfügung standen. Diese haben nur selten ein bestimmtes Allel unterscheiden können. Die Zuordnung eines serologischen Äquvalentes zu neuen Allelen erfolgt jetzt mittels Bioinformatik. In dem obigen Fall wäre es HLA-A2. Natürlich wäre auch hier von Vorteil, einen identen Spender zu nehmen, und das in der hohen Auflösung.
Das geht aber aufrund der hohen Diversität im HLA-System nicht. Einen identen Spender bei Stammzelltransplantation sucht man unter ca. 40 Millionen von gemeldeten Spendern weltweit. Bei Organtransplantationen "sucht" das Organ unter ca. 13.500 Patienten. Wenn man auch noch das Organ selbst berücksichtigt (der Patient ist zwar ident, braucht aber keine Niere, sondern ein Herz - und das kann von dem Spender nicht verwendet werden), wird es klar, warum es praktisch unmöglich ist, Organe HLA-ident zu transplantieren.
Bei SZT wird eine hohe Auflösung benötigt. Also auch dritte 3 und 4 Stelle muss definiert werden (in dem Fall gibt es sogar 3 Stellen). Also HLA-A*02:101 (4 digit, 2 Felder).
Das liegt daran, dass nach einer Stammzelltransplantation das Immunsystem des Spenders das des Empfängers ersetzt. Da aber alle anderen Gewebe im Körper noch immer die ursprüngliche
genetische Information tragen, kann das neue Immunsystem den Körper angreifen. Ausser bei eineigen Zwillingen passiert es leider - man nennt diese Komplikation nach der Stammzelltransplantation
die Graft versus Host Disease (GvHD).
Sie wird dadurch verursacht, dass maximal 12 Merkmale abgeglichen werden - es sind die wichtigsten, aber der Rest des Genoms bildet unzählige Unterschiede und diese werden von dem neuen Immunsystem erkannt und attackiert.
Zuletzt bearbeitet am 26.03.2024
